Es lo que se hace ahora con los antivirales y los kits de pruebas del virus. La Administración de Alimentos y Medicamentos (FDA) de EE. UU. está permitiendo su uso en los ámbitos clínicos, con la comprensión de que los medicamentos y las pruebas no se han evaluado del todo y se deben monitorizar de cerca para reunir datos sobre su efectividad.
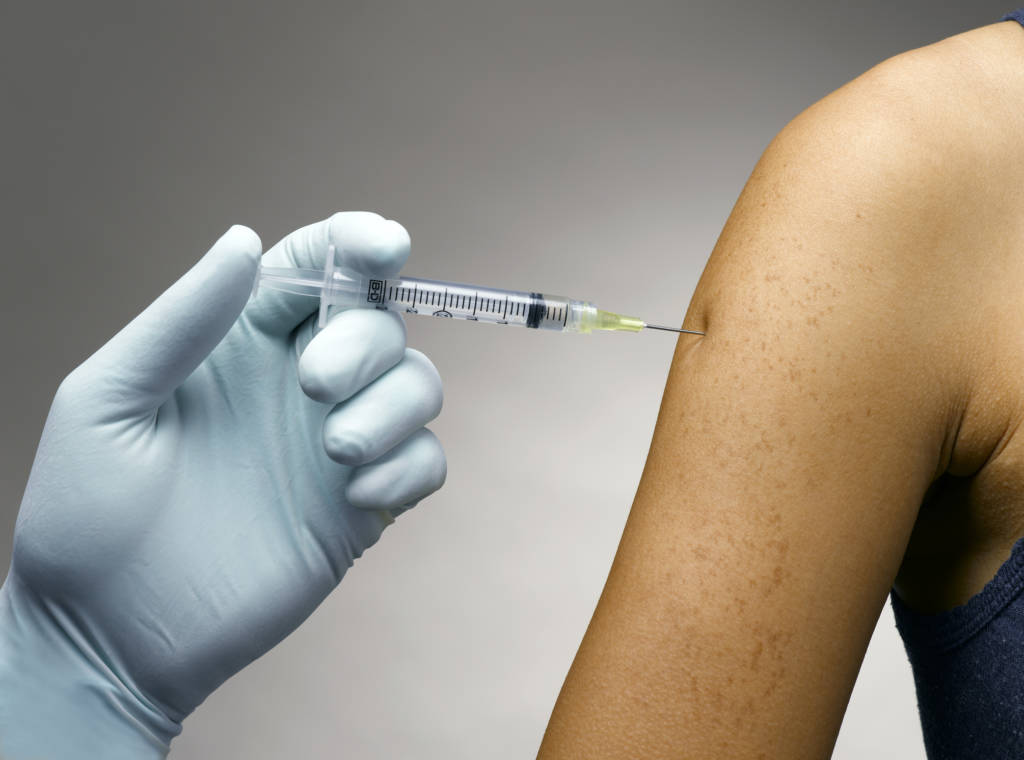
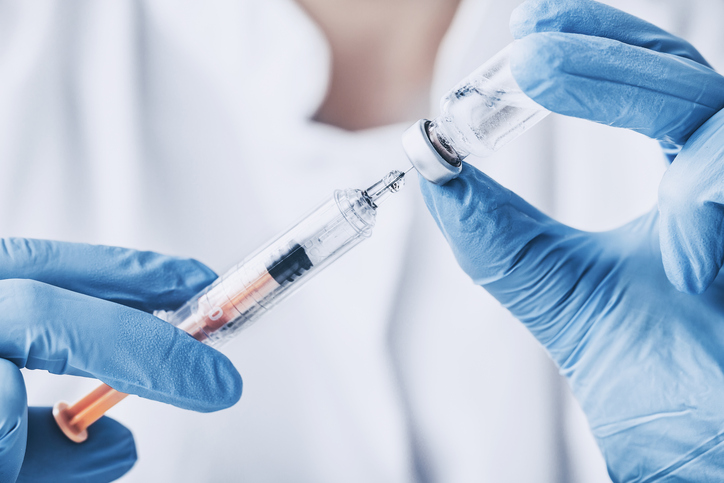
“Le administraremos una vacuna experimental, pero tiene que aceptar permitirnos tomar su temperatura, sacar sangre y evaluarlo”, planteó Poland. “Podríamos inmunizar a muchas personas con mucha rapidez, y básicamente ver qué sucede”, añadió.
“Creo que hay algunas personas dispuestas a hacer ese sacrificio”, dijo Poland. “Pero creo que hay muchas más personas que no están dispuestas a hacer ese sacrificio”.
El problema es el potencial de efectos secundarios peligrosos, como la amplificación de la infección dependiente de anticuerpos, una afección en que los anticuerpos formados en respuesta a la vacuna en realidad hacen que las infecciones futuras con el virus sean más graves.
“¿Qué sucede si se toma la vacuna, el virus muta, vuelve en otoño, y los que recibieron la vacuna en realidad ahora sufren un caso peor?”, preguntó Poland, anotando que este efecto ocurrió antes con una vacuna para el dengue y con una vacuna inactivada para el sarampión.
Tras la evaluación, el otro impedimento implica acelerar el proceso de fabricación, de forma que haya millones de dosis de una vacuna disponibles para el público, y se están tomando medidas para eliminar ese impedimento.
Respaldadas por fondos federales, compañías como Johnson & Johnson y Moderna están acelerando la producción de candidatos a vacunas no evaluados en lo que se conoce como sobre la base “de riesgos”.